La rhinite allergique et l’urticaire sont des maladies très courantes1 et pourtant leur impact est souvent minimisé ou ignoré.2
- La rhinite allergique et l’urticaire perturbent toutes deux la qualité de vie des enfants et des adolescents, entraînant des limitations dans les activités quotidiennes, ainsi que des problèmes émotionnels, pratiques et de sommeil. Par conséquent, ces maladies peuvent avoir un impact négatif sur la fréquentation et les résultats scolaires.1
Selon l’Académie européenne d’allergologie et d’immunologie clinique, la rhinite se caractérise par au moins deux des symptômes nasaux suivants : rhinorrhée, obstruction nasale, éternuements ou démangeaisons. Selon sa physiopathologie, on peut la classer en rhinite allergique, rhinite infectieuse ou rhinite non allergique et non infectieuse.2
De plus, la rhinite est souvent associée aux symptômes oculaires de la conjonctivite allergique (yeux rouges, larmoyants ou qui démangent, appelés prurit oculaire), donnant lieu à ce que l’on appelle la rhinoconjonctivite.2
La rhinoconjonctivite est fréquente chez les enfants et les adolescents en âge d’être scolarisés, avec une prévalence moyenne globale de 8,5 % chez les 6 à 7 ans et de 14,6 % chez les 13 à 14 ans. La prévalence de cette maladie semble augmenter, en particulier chez les adolescents.3
L’étude ISAAC (International Study of Allergies in Childhood) a conclu que dans un groupe de patients âgés de 6 à 7 ans, les filles présentaient généralement des troubles de rhinoconjonctivite moins fréquents que les garçons. En revanche, dans un groupe d’adolescents de 13 à 14 ans, les filles étaient plus fréquemment concernées que les garçons du même âge. En aucun cas, les résultats de l’étude n’ont varié en fonction de la région dans laquelle vivaient les patients.4
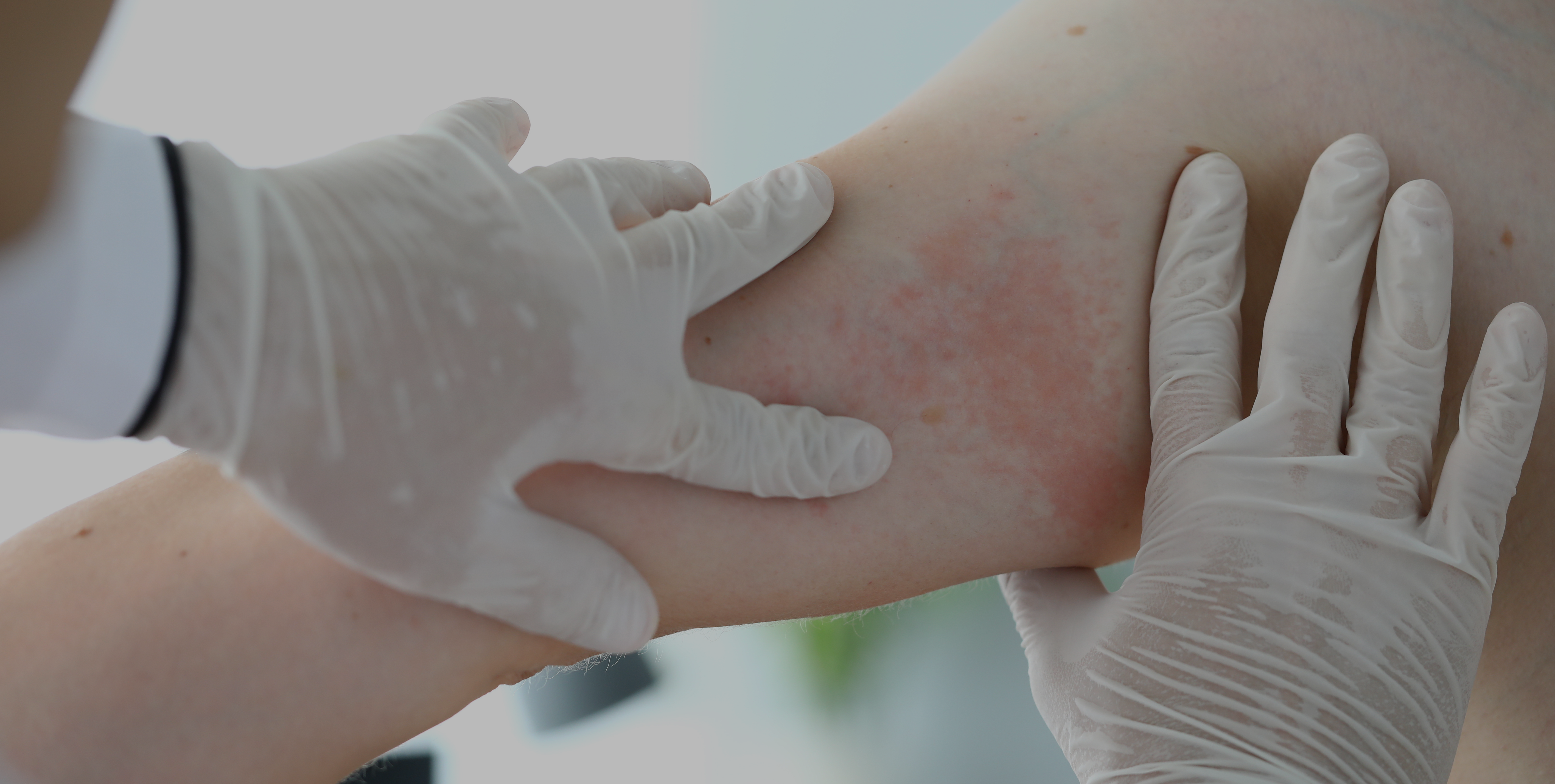
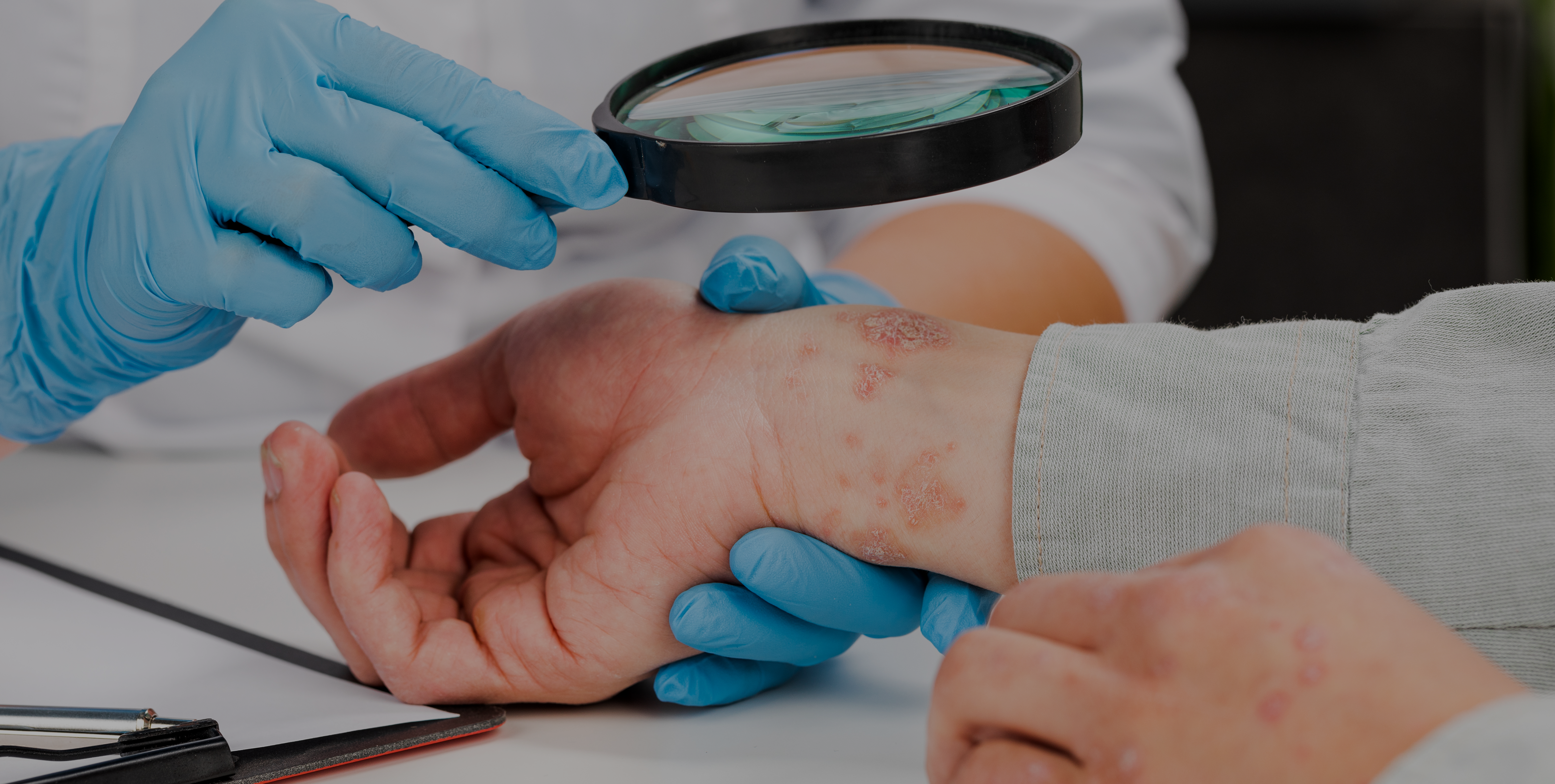
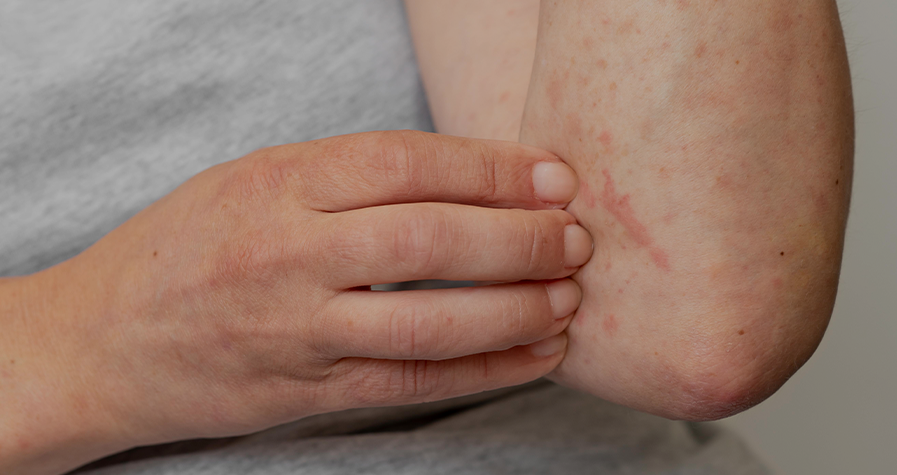
L’urticaire se caractérise par l’apparition de cloques ou de boutons très prurigineux (qui démangent), et elle a un impact important sur la qualité de vie des patients qui en souffrent.3 Il s’agit d’un trouble très répandu, puisqu’on estime que 15 à 24 % de la population globale en souffre à un moment donné de sa vie. Chez les enfants âgés entre 3 et 6 ans, jusqu’à 43,9 % de la population étudiée présentent de l’urticaire.5
Chez les enfants, contrairement aux adultes, l’urticaire aiguë (durée inférieure à 6 semaines) est plus fréquente (prévalence entre 1 % et 14 % chez les enfants) que la forme chronique ou persistante (prévalence entre 0,1 % et 1,8 % chez les enfants).1
L’urticaire aiguë est un processus d’apparition brutale qui peut persister quelques heures pouvant aller jusqu’à un maximum de 6 semaines.5 L’allergie alimentaire, l’allergie aux médicaments ou aux piqûres d’insectes, les infections virales, ainsi que tout ce qui peut déclencher une réaction cutanée immédiate sont les causes les plus courantes de l’urticaire aiguë.5,6
L’urticaire chronique peut être provoquée par un facteur déclenchant tel que le froid, la chaleur, l’eau, les frottements, etc., mais elle peut aussi apparaître spontanément sans que la cause soit identifiée. On estime qu’environ la moitié des urticaires chroniques durent moins d’un an, bien que dans 11 à 15 % des cas, la persistance dépasse 5 ans.5